cód. #3169
INEP - Química - 2019 - Exame Nacional do Ensino Médio - Primeiro Dia e Segundo Dia
Estudos mostram o desenvolvimento de biochips utilizados para auxiliar o diagnóstico de diabetes melito, doença evidenciada pelo excesso de glicose no organismo. O teste é simples e consiste em duas reações sequenciais na superfície do biochip, entre a amostra de soro sanguíneo do paciente, enzimas específicas e reagente (iodeto de potássio, KI), conforme mostrado na imagem.
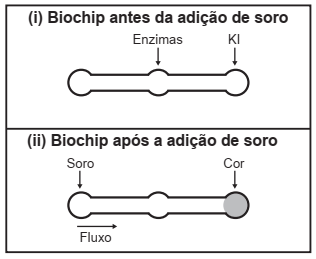
Após a adição de soro sanguíneo, o fluxo desloca- -se espontaneamente da esquerda para a direita (ii) promovendo reações sequenciais, conforme as equações 1 e 2. Na primeira, há conversão de glicose do sangue em ácido glucônico, gerando peróxido de hidrogênio:
Equação 1
C6H12O6 (aq) + O2 (g) + H2O (l)  C6H12O7 (aq) + H2O2 (aq)
C6H12O7 (aq) + H2O2 (aq)
Na segunda, o peróxido de hidrogênio reage com íons iodeto gerando o íon tri-iodeto, água e oxigênio.
Equação 2
2 H2O2 (aq) + 3 l− (aq) → I3− (aq) + 2 H2O (I) + O2 (g)
GARCIA, P. T. et al. A Handheld Stamping Process to Fabricate Microfluidic Paper-Based Analytical Devices with Chemically Modified Surface for Clinical Assays. RSC Advances, v. 4, 13 ago. 2014 (adaptado).
O tipo de reação que ocorre na superfície do biochip, nas duas reações do processo, é
A) análise.
B) síntese.
C) oxirredução.
D) complexação.
E) ácido-base.
A
B
C
D
E


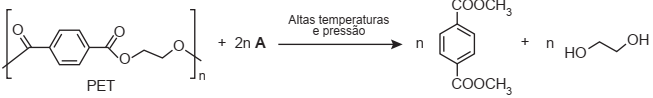

 C6H12O7 (aq) + H2O2 (aq)
C6H12O7 (aq) + H2O2 (aq)